- Accueil
- /Non classé
- /Réforme du circuit d’approvisionnement des produits de contraste
Réforme du circuit d’approvisionnement des produits de contraste
Mis à jour le 8 mars 2024
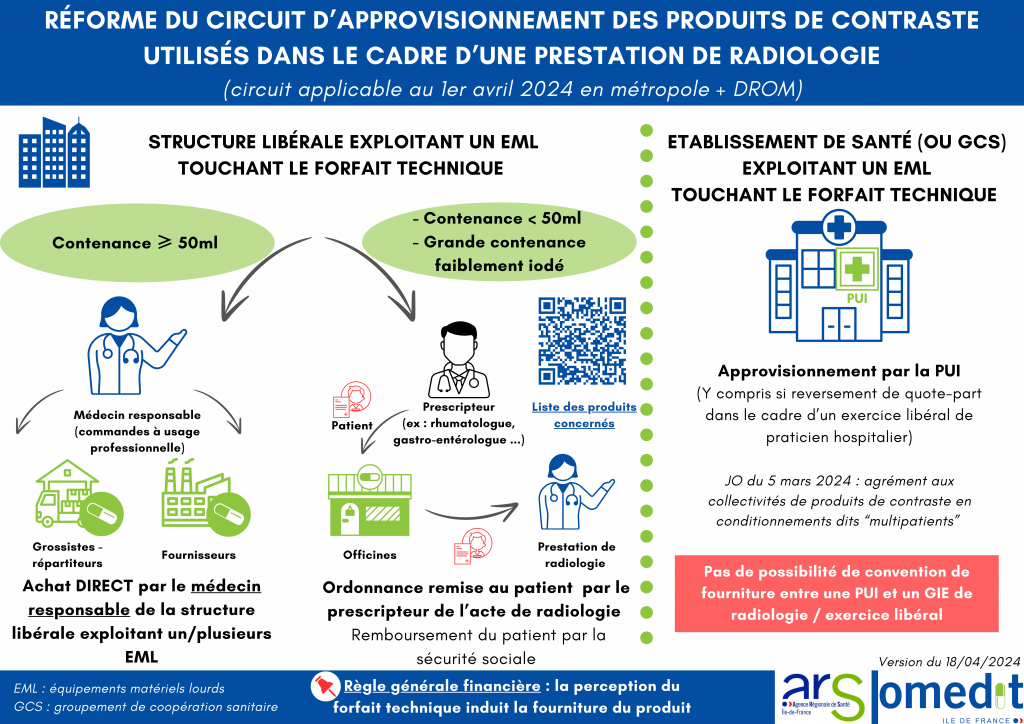
La réforme des produits de contraste est entrée en vigueur le 1er mars 2024 en métropole et dans les DROM (article 49 LFSS 2023 et article 59 LFSS 2024).
Elle modifie le circuit d’approvisionnement et les modalités de financement des produits de contraste utilisés en radiologie pour les scanners et les IRM.

- Les centres ou cabinets médicaux doivent désigner un médecin responsable.
- Celui-ci à la charge de commander les produits directement aux laboratoires ou via les officines (commandes à usage professionnel).
- Ils sont ensuite fournis directement aux patients pour la réalisation des examens d’imagerie médicale.
- La prise en charge par l’Assurance Maladie est assurée dans le cadre du forfait technique relatif à la réalisation de l’examen d’imagerie médicale.
- Le professionnel de santé prescrit l’ordonnance au patient.
- Celui-ci récupère les produits à l’officine.
- Le remboursement est ensuite effectué par la sécurité sociale directement au patient.
Les PUI assurent exclusivement l’approvisionnement en produits de contraste pour les services assurant cette activité pour les patients pris en charge par l’établissement (actes et consultations externes).
Par ailleurs, plusieurs produits de contraste en conditionnements dits “multipatients” ont reçu l’agrément aux collectivités au JO du 5 mars 2024.
A noter : Un double circuit de distribution des produits de contraste est mis en place durant une période transitoire d’un mois jusqu’au 31 mars 2024 afin d’éviter les interruptions de prise en charge des patients et les ruptures de stocks.
Voir également l’infographie du Ministère de la santé – Circuit pharmaceutique et logistique des produits de santé utilisés en radiologie
| Laboratoire | Code EAN / CODE CIP | Présentation | Substance / Principe actif |
| BAYER HEALTHCARE | 3400930080832 | GASTROGRAFINE ORAL RECT FL100ML BT 1 | sodium amidotrizoate méglumine amidotrizoate |
| BAYER HEALTHCARE | 3400930894668 | RADIOSELECTAN URIN. 30% INJ FL250ML BT 1 | méglumine amidotrizoate, sodium amidotrizoate |
| BAYER HEALTHCARE | 3400933090289 | ULTRAVIST 300 INJ FV20ML BT 1 | iopromide |
| BAYER HEALTHCARE | 3400933090630 | ULTRAVIST 370 INJ FV20ML BT 1 | iopromide |
| BRACCO IMAGING | 3400933791643 | IOMERON 150MG INJ FV250ML BT 1 | ioméprol |
| BRACCO IMAGING | 3400935469236 | IOMERON 300MG INJ FV20ML BT 1 | ioméprol |
| BRACCO IMAGING | 3400935469526 | IOMERON 350MG INJ FV20ML BT 1 | ioméprol |
| BRACCO IMAGING | 3400932458776 | IOPAMIRON 200MG INJ FL10ML BT 1 | iopamidol |
| BRACCO IMAGING | 3400932458837 | IOPAMIRON 300MG INJ FL10ML BT 1 | iopamidol |
| BRACCO IMAGING | 3400935756466 | SONOVUE 8MCL/ML INJ FL+SRG BT 1 | soufre hexafluorure |
| GE HEALTHCARE | 3400933846336 | VISIPAQUE 270MG INJ FV20ML BT 1 | iodixanol |
| GUERBET | 3400930265543 | ARTIREM 0,0025mmol/ml solution injectable en flacon verre (B/1) | acide gadotérique |
| GUERBET | 3400930674994 | MICROPAQUE ORAL FL150ML BT 1 | baryum sulfate |
| GUERBET | 3400930675076 | MICROPAQUE RECT FL500ML BT 1 | baryum sulfate |
| GUERBET | 3400933053901 | MICROPAQUE SCANNER BUV FP150ML BT 1 | baryum sulfate |
| GUERBET | 3400931716013 | TELEBRIX 12 (SODIUM 120) FV250ML BT 1 | acide ioxitalamique sel de Na |
| GUERBET | 3400932748150 | TELEBRIX GASTRO 300 FV100ML BT 1 | acide ioxitalamique sel de méglumine |
| GUERBET | 3400926907990 | XENETIX 300 INJ FV20/20ML BT 1 | iobitridol |
| GUERBET | 3400926908362 | XENETIX 350 INJ FV20/20ML BT 1 | iobitridol |
| GUERBET | 3400955002109 | MICROPAQUE FL2000ML BT 1 | baryum sulfate |
Sources : laboratoire BAYER HEALTHCARE, BRACCO IMAGING, GE HEALTHCARE & GUERBET
La procédure de sérialisation visant à lutter contre l’introduction de médicaments falsifiés dans la chaine d’approvisionnement (dispositif d’inviolabilité et identifiant unique sur les boîtes) ne s’applique pas aux produits de contraste.
En cas de décision de rappel de lot convenue avec l’ANSM, en vertu des articles R. 5124-2 et R. 5124-45 du code de la santé publique, il appartient aux exploitants des spécialités concernées de prendre toute mesure utile en matière de communication et de s’assurer de la bonne diffusion de l’information du rappel aux cabinets de radiologie et aux autres praticiens concernés et du retour de toutes les unités vendues, en cours de livraison, et non consommées.
Il convient en outre de prendre en compte, lors de cette procédure de rappel de lots, l’ensemble des médicaments ayant fait l’objet de ce rappel qu’ils soient stockés au sein d’un établissement pharmaceutique, d’une officine de pharmacie, d’une pharmacie à usage intérieur, par des structures ou des professionnels visés aux articles R. 5124-44- et R. 5124-45 ou ceux en cours de livraison. Par ailleurs, jusqu’à l’administration au patient, l’ensemble des acteurs de la chaine de distribution doit veiller à l’effectivité du retrait des lots ayant fait l’objet d’un rappel en se basant sur l’ensemble des données de traçabilité dont ils disposent.
En pratique, les laboratoires devront informer les cabinets de radiologie et autres praticiens concernés par l’achat de produits de contraste, par messagerie électronique en utilisant les coordonnées du médecin responsable désigné de la structure ou celles du praticien ayant passé une commande à usage professionnel et en lui joignant les instructions à suivre sur les modalités de rappel.
Légifrance – JO de radiation de certains médicaments, nécessaires à la réalisation d’examens d’imagerie médicale, de la liste des spécialités remboursables aux assurés sociaux (Texte n° 12, Texte n° 13, Texte n° 14, Texte n° 15)